– riaditeľ Inštitútu du Col, Paríž
– prezident organizácie EUROGIN ( European Research Organization on Genital Infection and Neoplasia )
– prezident medzinárodnej nadácie WACC ( Women Against Cervical Cancer )
Existujú silné dôkazy o tom, že HPV infekcia je síce nevyhnutným, nie však jediným faktorom nutným pre vývoj prekarceróznych lézií krčka maternice. V súčasnosti je známy vysoký počet typov HPV, ale len u zlomku z tohto počtu bol skutočne potvrdený onkogénny potenciál. Pätnásť z nich je považovaných za vysoko rizikových z hľadiska vzniku karcinómu krčka maternice. S mierou najvyššieho rizika je priamo spojených päť typov ( 16, 18, 31, 33, 45 ). V prípade typov 16 a 18 je to 60 % CIN3 a 70 % karcinómu ( pozn. prekl. : CIN 3 je možné považovať za závažný stupeň, zodpovedá ťažkej dysplázii ). Tradičný pohľad na ochorenie je potrebné v plnom rozsahu prehodnotiť so zreteľom na vysoko rizikové pôsobenie najaktívnejším typom HPV.
Prenos infekcie sa deje všetkými spôsobmi sexuálneho styku. Najcitlivejšou a najzraniteľnejšou oblasťou je pritom hrdlo maternice a to zrejme vďaka tomu, že jeho transformačná zóna je ľahko prístupná kontaktu s vlastným vírusom ( pozn. prekl.: transformačná zóna je pásmo epiteliálnej premeny; prebieha tu metaplastický proces premeny cylindrického v dlaždicovitý epitel a je v všeobecne náchylnejší k onkogénnym zmenám ). V priebehu života riziko priameho kontaktu s HPV dosahuje u žien až 70 % hranice a celoživotné riziko vzniku karcinómu krčka maternice sa odhaduje medzi 0,6 – 3 %.
Najvyššia prevaha HPV infekcie je medzi 20 – 25 rokom, kedy dosahuje úroveň 30 %, so stúpajúcim vekom potom postupne klesá až na rozhranie 10 – 12 %. Mladé ženy predstavujú skupinu s najväčšou mierou rizika. Svoju rolu môže zohrať vyššia expozícia vírusu vďaka častejšiemu striedaniu sexuálnych partnerov, nezrelosť metaplastického epitelu transformačnej zóny a určitá nedostatočnosť imunitných obranných mechanizmov. Napriek tomu môže byť v niektorých prípadoch vlastná infekcia prechodná a spontánne odznie v rozmedzí 18 – 36 mesiacov, najmä ak je spôsobená menej aktívnym typom vírusu.
Vymiznutie vírusu je možné pripísať na vrub činnosti prirodzenej imunity, ale i ďalším – doposiaľ nie úplne jasným – mechanizmom. Jednako prirodzená imunita sama o sebe nezaisťuje celoživotnú ochranu a opakovaná nákaza dokonca rovnakým typom vírusu je ľahká. HPV infekcia teda sama o sebe neimunizuje organizmus, nutná je vakcinácia ( pozn. prekl.: očkovanie je účinné len na určité typy vírusov a i tak sa môže reinfekcia objaviť).
Najvýznamnejším indikátorom lézií je vytrvalosť vírusu. Kumulatívne riziko CIN3 u pretrvávajúcej infekcie HPV typom 16 v dĺžke presahujúcej 10 rokov je 50 % . Medzi markery perzistencie je uvádzaný rad faktorov vrátane veku, fajčenia, prítomnosti chlamýdiových infekcií, perorálnej antikoncepcie i imunosupresie ( pozn. prekl.: imunosupresiu môžu navodiť niektoré liečivá ). Tie isté faktory potom predstavujú riziko vzniku karcinómu krčka maternice. Napr. v membránach buniek epitelu krčka maternice bol zistený nikotín s jeho metabolitmi, samotné fajčenie má negatívny vplyv na lokálne imunitné mechanizmy. Ženské pohlavné hormóny svojim efektom na bunkovú proliferáciu môžu indukovať citlivosť k poškodeniu DNA cieľových buniek.
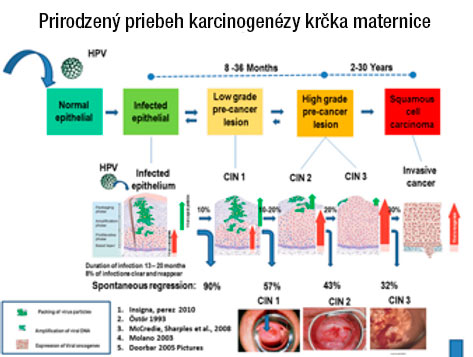
Výsledkom dlhodobej expozície HPV, predovšetkým však vyššie spomínaným najaktívnejším typom, je vývoj karcinómu v oblasti hrdla maternice. Morfologickým podkladom infekcie môžu byť nízko stupňové (LSIL) lézie, ktoré ešte môžu prejsť regresom a spontánne vymiznúť vďaka postupne sa rozvíjajúcimi obrannými reakciami imunitného systému. Vysoko stupňové lézie (HSIL) sú všeobecne považované za zmenu s vysokou mierou rizika postupného progresu na karcinóm. Observačné štúdie ukazujú, že doba potrebná k tomu, aby pretrvávajúca HPV infekcia prešla cez začínajúce zmeny transformačnej zóny až po samotný karcinóm dosahuje 15 – 20 rokov. Sú však známe i kratšie intervaly tohto progresu. Špecifické mechanizmy tohoto prechodu sú s najväčšou pravdepodobnosťou výsledkom interakcie vírusového agens s prirodzenou imunitou hostiteľa, ktorého jednotlivé zložky nie sú úplne známe. Vznikajúca imunitná reakcia je pravdepodobne sprostredkovaná lokálnymi dejmi vrodenej imunity s účasťou prirodzených likvidátorov (natural killer cells, NK-bunky) a aktiváciou receptorov toll-like (pozn. prekl.: toll-like receptory boli najprv objavené u lariev mušky drozofily obyčajnej, kde sa môžu podieľať na poruchách larválneho vývoja – odtiaľ „toll“ v zmysle zmätený). Pokračujúca prítomnosť vírusu pravdepodobne vedie k adaptívnej imunitnej reakcii založenej na aktivite antigén- prezentujících buniek s účasťou ako prirodzenej ( vrodenej ), tak získanej ( adaptívnej ) zložky imunity. Po preniknutí vírusu dochádza k jeho kontaktu s bazálnymi bunkami, jedná sa omnipotentné bunky, ktoré sú citlivé na virión v oblasti skvamokolumnárnej junkcie (poz. prekl.: jedná sa o hranice medzi dlaždicovým epitelom hrdla maternice a žľazovým endocervikálnym epitelom). Dochádza tu k expresii a dozrievaniu génov proteínov L1 a L2 (pozn. prekl.: L1 je hlavný štrukturálny proteín vírusového „obalu“ – kapsidy; L2 je proteín kompletizujúci samotný virión inkorporáciou vírusového genetického materiálu do DNA hostiteľskej bunky).
Pôsobením vírusových onkoproteínov E6 a E7 sa pôvodne diferencovaný epitel LSIL lézie postupne transformuje na stále menej a menej diferencovaný epitel HSIL ( pozn. prekl.: protín E6 inaktivuje mechanizmy zaisťujúce integritu hostiteľskej bunky; E7 inaktivuje bunečný proteín pRb, ktorého fyziologickou funkciou je tlmiť nekontrolovateľné bunkové delenie ). Onkoproteíny E6 a E7 zasahujú do cyklu bunkového delenia narušením funkcie regulačných proteínov p53 a pRb (pozn. prekl.: proteín p53 má radu funkcií, mimo iných aj stimuluje proces diferenciácie buniek a zahájenie apoptózy). Bunka sa dôsledkom toho stáva nestabilnou a vírus tak dosahuje v LSIL lézii schopnosť ďalšieho šírenia, v HSIL lézii je – pokiaľ je známe – v epizomálnom stave (pozn. prekl.: epizomálny – mimo bunkové chromozómy; epizomálne štádium je typické pre latentný priebeh infekcie a preto nedochádza k ich klinickým prejavom). V LSIL lézii dochádza k dokončeniu obnovenia vírusu, z epizomálneho štádia v HSIL lézii môže byť včlenený do genómu hostiteľskej bunky a dochádza k vzniku nádorovej bunky.
Mikrobióm a HPV
Mikrobióm všeobecne hrá dôležitú úlohu v ľudskom zdraví. Je známe, že dysbalancia v rámci mikrobiómu sa môže podieľať na vzniku karcinómu hrubého čreva či atopickej dermatitídy. Hlavnou zložkou mikrobiómu vagíny je početná skupina baktérií Lactobacillus acidophillus, ktorých zloženie a vzájomný pomer môžu ovplyvňovať stav lokálnej imunity.
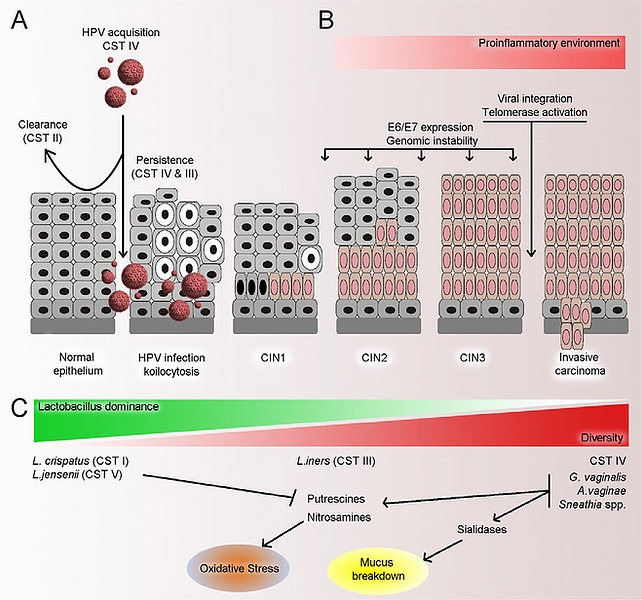
Metódami in vitro bolo zistené, že niektoré laktobacily ( Lactobacillus spp. ) majú cytostatický efekt na nádorové bunky karcinómu krčka maternice. Ukazuje sa, že medzi mikrobiotmi, látkami nimi produkovanými a bunkami krčka maternice existujú vzájomné interakcie. Existujú aj dôkazy o možnosti ovplyvňovania HPV infekcie aktuálnym stavom pošvovej mikroflóry.
Metaanalýzou celkom 12 klinických štúdií bola potvrdená pozitívna korelácia medzi HPV infekciou a súčasnou prítomnosťou bakteriálnej vaginózy. Deplécia bacilov podporuje perzistenciu HPV infekcie. Zistilo sa, že ženy s pretrvávajúcou HPV infekciou mali v 11% prevahu vaginózy v porovnaní s 5% prevahou u žien bez HPV. U žien s vaginózou došlo tiež k predĺženiu času potrebného k spontánnemu vymiznutiu HPV ( pomer rizík – hazard ratio HR = 0,84; 95% Cl 0,72 – 0,97 ). Jedna z prvých štúdií vyšetrujúcich vzťah pošvového mikrobiómu a HPV bola prevedená v Kórei. Bolo analyzovaných 68 pacientok, z ktorých 23 vykazovalo HPV pozitivitu a 45 bolo HPV negatívnych. HPV-pozitívne ženy mali vyššiu rôznorodosť mikrobiómu s nižším podielom Lactobacillus spp. v porovnaní s HPV- negatívnymi. Analýza tiež ukázala, že určité baktérie (fusobaktérie, predovšetkým Prevotella) je možné využiť ako mikrobiologický marker HPV infekcie.
Hoci vyššie uvedené fakty ukazujú na dôležitosť mikrobiómu pri modulácii imunitnej reaktivity ženských pohlavných ciest, rad otázok stále čaká na odpoveď:
– môže zloženie mikrobiómu vyskytujúceho sa súčasne s nediferencovanou skvamóznou metapláziou u mladých žien vysvetliť vyšší výskyt HPV infekcie v tomto veku?
– majú rizikové faktory, ako je fajčenie, imunosupresia, perorálna antikoncepcia, negatívny vplyv na také zmeny mikrobiómu, ktoré by podporovali proces kancerogenézy?
– sú vekovo závislé rozdiely v prevalencii HPV, HSIL a cervikálneho karcinómu výsledkom zmien zloženia mikrobiómu?
– môžu naopak HPV infekciami indukované zmeny v zložení mikrobiómu spustiť onkogénne faktory vedúce ku kancerogenéze?
– Záver –
Záverom je možné povedať, že pošvový mikrobióm má zrejme význam pri nákaze a perzistencii HPV infekcie, vrátane jej progresie do vyšších štádií CIN. Pre potvrdenie tohoto predpokladu však budú nutné ďalšie štúdie zamerané na skúmanie súvislostí zloženia a diverzity mikrobiómu s klinickými prejavmi.
Získané poznatky tak môžu poskytnúť príležitosť k vývoju nových liečiv cielených na zachovanie a obnovenie pošvového mikrobiómu, mohlo by sa napr. jednať o špecifické probiotiká , bioselektívne substráty podporujúce rast laktobacilov zabraňujúcich vzniku a vývoju prekancerogénnych lézií.
– starší konzultant odboru ženskej onkológie,
– súkromný lekár,
– bývalý prezident Španielskej asociácie cervikálnej patológie a kolposkopie
– prezident EUROGIN 2015
Cieľom tejto správy je posúdenie prospešnosti prípravku Papilocare® so zvlhčujúcimi a regeneračnými účinkami na vaginálnu sliznicu vo vzťahu k re-epitelizačnej funkcii v prípadoch, keď dochádza k mikrotraumám sliznice. Týmto spôsobom prípravok zabraňuje integráciu vírusu do buniek a predchádza tak HPV infekcii.
Štúdium Cleopatra l zistilo priemernú početnosť HPV infekcie u celého súboru žien vo veku medzi 18 – 68 rokov vo výške 14 %, pritom v skupine s vekovým rozmedzím 18 – 30 rokov sa početnosť pohybovala na stabilnej úrovni 30 % , vo veku 30 – 35 rokov potom došlo k poklesu na úroveň pohybujúceho sa okolo 10 %. Na základe týchto výsledkov je možné povedať, že v Španielsku je v priebehu prvej tretiny života žien prítomnosť HPV v pošvovej sliznici bežná. Z dôvodu stále väčšieho počtu známych príčin (mimo iného typ vírusu, aktuálny stav obranyschopnosti organizmu hostiteľa ) existuje možnosť spontánneho vymiznutia infekcie s výnimkou určitej skupiny žien, kedy k tomu nedochádza. Túto skupinu je možné charakterizovať ako chronické prenášačky HPV. Práve u týchto žien sme nútení predpokladať existenciu vysokého rizika začiatočného vývoje prekanceróznych lézií v oblasti krčka, ktoré môžu vo vysokom percente viesť k vývoju invazívneho karcinómu v tejto oblasti. Vysoké riziko samozrejme ešte neznamená absolútnu istotu. Na základe zdokumentovaných invazívnych karcinómov sa ukázalo, že len u obmedzeného počtu žien došlo k vývoji CIN3. Prečo tomu tak je?
– Patogenéza HPV infekcie –
Vyššie uvedené úvahy týkajúce sa procesu infekcie sme v nedávnej dobe doplnili o vlastné poznatky. Aj keď je to veľmi jednoduché, je nutné mať na pamäti, že číra prítomnosť HPV v cervikálnej či análnej mukoidnej tekutine nemusí ešte znamenať vlastnú HPV infekciu. Byť skutočne nakazenou predstavuje ďalší krok, ktorý znamená, že došlo k integrácii samotného vírusu, tzn. k jeho presunu z tekutiny do vlastného epitelu krčka maternice a postupnému ovládnutiu cieľových buniek. Existuje preto stále viac dôkazov o prospešnosti techník k preukazovaniu vírusovej mRNA a expresie onkogénov E6 a E7, ktoré sú zároveň markery integrácie vírusu do genómu napadnutej bunky a teda i samotného zahájenia onkogénneho procesu. Krčok maternice sám o sebe predstavuje nestabilnú histologickú štruktúru, kde sa neustále stretáva rozhranie dvoch epitelov a to vrstevnatého dlaždicovitého epitelu časti krčka vykleňujúceho sa do pošvy (pozn.: ektocervix) a jednovrstvového cylindrického žľazového epitelu maternicového kanálu (pozn.: endocervix). Pod cylindrickým epitelom sa nachádza línia rezervných buniek, ktoré si zachovávajú schopnosť rastu a následnej diferenciácie a to najčastejšie do zrelých foriem buď skvamózneho alebo žľazového epitelu.
Pri delení rezervných buniek dochádza v priebehu pohlavného vývoja ženy k ich bujneniu a poklesu endocervikálneho epitelu smerom navonok (tj. do ektocervixu). Žľazový epitel sa vplyvom odlišného prostredia vagíny mení na epitel dlaždicový. Vo svojej podstate sa jedná o normálny proces, ktorý prebieha u každej sexuálne aktívnej ženy a je stimulovaný i užívaním perorálnej antikoncepcie, zavedením vnútromaternicového telieska, či prostým tehotenstvom. HPV potrebuje k svojej integrácii mitotickú aktivitu buniek. Túto podmienku spĺňajú práve rezervné bunky v štádiu metaplastickej re-epitelizácie a predstavujú tak ideálny cieľ pre ukotvenie vírusu. Z toho vyplýva, že na druhej strane dobre epitelizovaný cervix so skvamóznym (= spinocelulárním) epitelom a obmedzeným prolapsom ( poklesnutím ) transformačnej línie či jej neprítomnosťou je menej vhodným prostredím pre kolonizáciu vírusov i onkogénny potenciál HPV infekcie.
Papilocare®
možnosť preventívnej stratégie
Máme dôkazy potvrdzujúce, že vaginálny gél Papilocare® podporuje re-epitelizáciu cervixu. Predpokladáme preto, že jeho prostredníctvom je možné obmedziť integráciu vírusu zmenšením citlivej oblasti epitelu s intenzívnou mitotickou aktivitou, ktorá inak predstavuje dokonalé miesto integrácie HPV. V tomto prostredí sa tak možnosť ukotvenia HPV s onkogénnym potenciálom významne znižuje.
– Záver –
S ohľadom na vyššie uvedené fakty a na základe vlastných výsledkov súhlasím s tým, že „bariérový efekt“ vyvolaný Papilocare® oprávňuje uvažovať o možnostiach jeho použitia u pacientiek s narušenou cervikálnou epitelizáciou, čo zabraňuje integrácii vírusu a rozvoju HPV infekcie.
